Руководитель проекта
Руководитель проекта – Бокерия Лео Антонович, Академик РАН, Заслуженный деятель науки России, директор НЦССХ им. А. Н. Бакулева. МР cистема – Achieva 3T TX, R5.1.
Темы совместных научных проектов
Комплексная оценка сердца и сосудов у пациентов со сложными врожденными пороками сердца и некоронарогенными поражениями миокарда.

T1-картирование (MOLLI) и оценка степени фиброза при поражении миокарда
Цель: Апробация и внедрение в клиническую практику новейших техник количественной оценки степени фиброза при инфаркте миокарда, основанных на применении методики MOLLI. Описание проекта: Фиброз миокарда связан с пролиферацией фибробластов в сердечной мышце, что делает ее менее эластичной и приводит к сердечной недостаточности. Молекулярные механизмы развития фиброза могут быть разными при разных заболеваниях, и до сих пор изучены недостаточно [1-2]. Можно выделить разные степени развития заболевания [3]: от начальной стадии межклеточного фиброза до необратимого замещающего фиброза (Рис.1). Своевременная диагностика и лечение позволяют предотвратить развитие заболевания.
Разработка МРТ методики оценки перфузии легких при легочной гипертезии
Цель: Разработка и клиническая апробация техники количественной оценки кровоснабжения легких. Описание проекта: Для легочной гипертензии характерно повышенное давление крови в сосудах, что приводит к изменению стенки сосуда, снижению кровотока, гипертрофии правого желудочка и сердечной недостаточности правых отделов сердца. При врожденных пороках сердца для планирования лечения необходима оценка кровоснабжения легких. В настоящее время наиболее информативной является методика SPECT/CT. Однако, разработка неинвазивной МРТ технологии оценки легочной гипертензии и функции сердца представляет значительный интерес всвязи с отсутствием в исследовании ионизирующего излучения и возможности получения различных типов контрастов для оценки структурных и функциональных изменений, а также меньшей стоимостью исследования. Результаты: На основе Т1ВИ и методик с ультракоротким TE разработаны прототипы методики исследования функции легких.
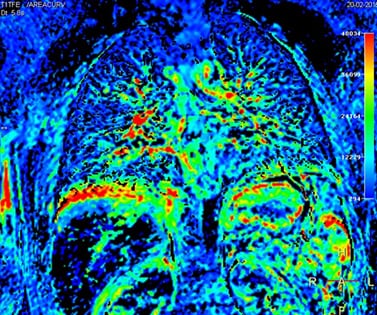
Рис. 3А. Цветная карта перфузии легких, полученная при свободном дыхании пациента.
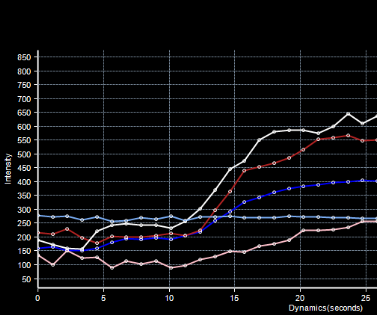
Рис. 3Б. Кривая перфузии легких – зависимость интенсивности МР сигнала ткани легких от времени при болюсном введении контрастного вещества.

Последние новости и события